
- Yazar Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Son düzenleme 2025-01-22 17:12.
klor izotop 18 nötron ile 0.7577 bolluğa ve 35 amu kütle numarasına sahiptir. hesaplamak için ortalama atom kütlesi, kesri her biri için kütle numarasıyla çarpın izotop , sonra bunları birlikte ekleyin.
Benzer şekilde, bir elementin tüm izotoplarının ağırlıklı ortalaması nedir?
Farklı kitlelerin kullanılması izotoplar ve her biri ne kadar bol izotop olduğunu, bulabiliriz ortalama bir atomun kütlesi eleman . Atom kütlesi bir eleman bu ağırlıklı ortalama doğal olarak oluşan bir numunedeki atomların kütlesi eleman . Atom kütlesi tipik olarak atomik kütle birimlerinde rapor edilir.
1 amu'luk bir kütleye sahip olan nedir? Bir atomik kütle birimi (sembolize edilmiş AMU veya amu), bir karbon-12 atomunun kütlesinin tam olarak 1/12'si olarak tanımlanır. Karbon-12 (C-12) atomunun altı tane protonlar ve altı nötronlar çekirdeğinde. Kesin olmayan terimlerle, bir AMU, proton dinlenme kütlesi ve nötron dinlenme kütlesi.
İkincisi, atom kütlesini kullanarak bolluk yüzdesini nasıl hesaplarsınız?
Her birini değiştir yüzde bolluk 100'e bölerek ondalık biçime getirin. Bu değeri atom kütlesi bu izotopun. Ortalamayı elde etmek için her izotop için bir araya getirin atom kütlesi.
Atom kütlesi ile atom ağırlığı arasındaki fark nedir?
atom kütlesi (ma) kitle bir atom . Bir tek atom belirli sayıda proton ve nötrona sahiptir, bu nedenle kitle kesindir (değişmez) ve proton ve nötron sayısının toplamıdır atomda . Atom ağırlığı ağırlıklı ortalamasıdır kitle hepsinden atomlar izotopların bolluğuna bağlı olarak bir elementin
Önerilen:
Ağırlıklı ortalamayı nasıl yorumluyorsunuz?

Özet. Ağırlıklı Ortalama: Bazı değerlerin diğerlerinden daha fazla katkıda bulunduğu ortalama. Ağırlıklar 1'e eklendiğinde, her ağırlığı eşleşen değerle çarpın ve hepsini toplayın. Aksi takdirde, her w ağırlığını eşleşen değeri x ile çarpın, hepsini toplayın ve ağırlıkların toplamına bölün: Ağırlıklı Ortalama = ΣwxΣw
Excel'de nüfus ortalamasını nasıl hesaplarım?
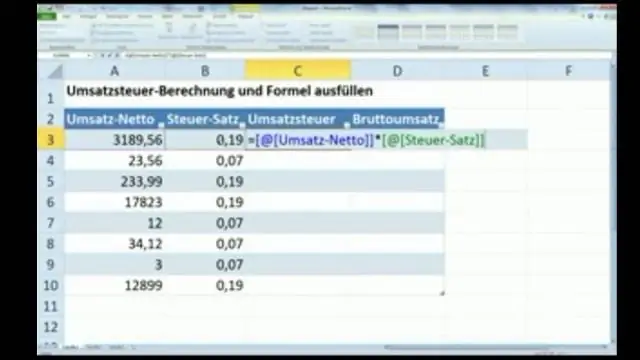
Nüfus Ortalaması = Tüm Maddelerin Toplamı / Madde Sayısı Nüfus Ortalaması = (14+61+83+92+2+8+48+25+71+12) / 10. Nüfus Ortalaması = 416 / 10. Nüfus Ortalaması = 41,6
Bir koordinat düzleminde bir genişlemenin ölçek faktörünü nasıl buluyorsunuz?
ABC üçgenini A(2, 6), B(2, 2), C(6, 2) koordinatlarıyla çizin. Ardından görüntüyü, genişleme merkezi olarak orijin ile 1/2 ölçek faktörü kadar genişletin. İlk önce orijinal üçgenimizi koordinat düzleminde çiziyoruz. Ardından, her koordinatı 1/2 ölçek faktörü ile çarpıyoruz
Pivot tabloda ağırlıklı ortalama nasıl oluşturulur?

PivotTable'da Ağırlıklı Ortalamalar PivotTable araç çubuğunun sol tarafındaki PivotTable kelimesinin yanındaki aşağı oku tıklayın. Formülleri Seç | Hesaplanan Alanlar. Ad kutusuna yeni alanınız için bir ad girin. Formül kutusuna, ağırlıklı ortalamanız için kullanılmasını istediğiniz formülü, örneğin =AğırlıklıDeğer/Ağırlık gibi girin. Tamam'ı tıklayın
Bir nokta ve bir paralel çizgi verilen bir çizginin denklemini nasıl buluyorsunuz?
Doğrunun eğim-kesme noktası formundaki denklemi y=2x+5'tir. Paralel doğrunun eğimi aynıdır: m=2. Yani paralel doğrunun denklemi y=2x+a'dır. a'yı bulmak için, doğrunun verilen noktadan geçmesi gerektiği gerçeğini kullanırız:5=(2)⋅(−3)+a
