
İçindekiler:
- Yazar Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Son düzenleme 2025-01-22 17:12.
Öğeye göre yüzde bileşimi
| eleman | Sembol | Kütle Yüzdesi |
|---|---|---|
| Hidrojen | H | 5.037% |
| Azot | n | 34.998% |
| Oksijen | Ö | 59.965% |
Basitçe, nh4no3'teki nitrojen kütlesi yüzdesi nedir?
Cevap ve Açıklama: kütle yüzdesi ile ilgili azot amonyum nitratta aşağıda gösterilen ifade ile hesaplanabilir. sayısının değerlerini değiştirin n -atomlar, N'nin kütlesi -atom ve N'nin kütlesi H4 n O3 n H4 n Yukarıdaki denklemde O3. bu yüzden yüzde tarafından azot kütlesi amonyum nitratta %34.999'dur.
Ayrıca amonyum nitratta ne kadar azot olduğu da sorulabilir. Amonyum nitrat NPK derecesi 34-0-0 (%34) ile önemli bir gübredir azot ). Üreden (46-0-0) daha az konsantredir, amonyum nitrat hafif bir ulaşım dezavantajı.
Ayrıca, amonyum nitrattaki azotun kütlece yüzdesini nasıl hesaplarsınız?
Açıklama:
- 2×14g=28g. N'nin kütlesi 28g'dir. N'nin yüzde bileşimi 28g80g×%100=%35'tir.
- 4×1g=4g. H'nin kütlesi 4g'dir. H'nin yüzde bileşimi 4g80g×%100=%5'tir.
- 3×16g=48g. O'nun kütlesi 48g'dir. O'nun yüzde bileşimi 48g80g×%100=%60'tır.
Amonyum nitratın formül kütlesi nedir?
80.043 g/mol
Önerilen:
İki atomlu azotun formülü nedir?

Cevap ve Açıklama: Azot, iki atomlu bir molekül örneğidir. Azot gazının kimyasal formülü N2'dir. Diğer iki atomlu moleküller hidrojen, oksijen
Bu yapıdaki azotun formal yükü nedir?

Azotla devam edersek, (a)'da azot atomunun üç bağ çifti paylaştığını ve bir yalnız çifti olduğunu ve toplam 5 değerlik elektronuna sahip olduğunu gözlemliyoruz. Bu nedenle nitrojen atomu üzerindeki formal yük 5 - (2 + 6/2) = 0'dır. (b)'de nitrojen atomunun formal yükü -1'dir
Bir protonun kütlesi ile bir elektronun kütlesi arasındaki fark nedir?
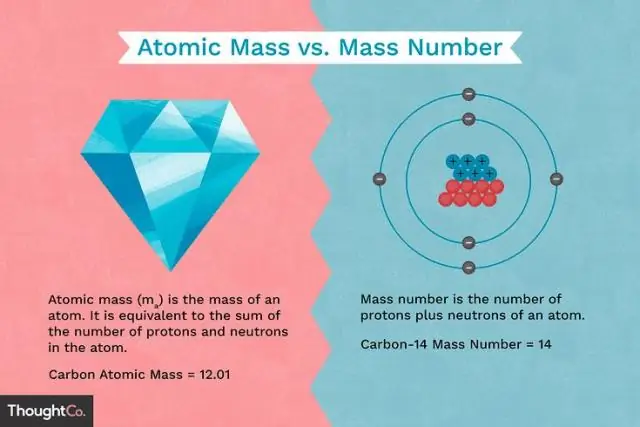
Protonlar ve nötronlar yaklaşık olarak aynı kütleye sahiptir, ancak ikisi de elektronlardan çok daha büyüktür (bir elektronun yaklaşık 2.000 katı). Proton üzerindeki pozitif yük, elektron üzerindeki negatif yüke eşit büyüklüktedir
Azotun iyonlaşma enerjisi kJ mol nedir?

Moleküler azotun iyonlaşma enerjisi 1503 kJ mol?-1, atomik azotunki ise 1402 kJ mol?-1'dir. Bir kez daha, moleküler nitrojendeki elektronların enerjisi, ayrılmış atomlardaki elektronlarınkinden daha düşüktür, bu nedenle molekül bağlanır
Azotun Amu'su nedir?

Azot 7 numaralı elementtir. Bu periyodik tabloyu kullanarak, azotun atom kütlesinin 14.01 amu veya 14.01 g/mol olduğunu görüyoruz
